






Malgré un paysage très complexe, l’étude de nouveaux biomarqueurs élargit notre vision de la physiopathologie du cancer gastrique, et l’analyse des biomarqueurs pourrait offrir une meilleure compréhension de cette maladie.


CLDN18.2 : claudine 18.2; FGFR2b : récepteur 2b du facteur de croissance des fibroblastes (fibroblast growth factor receptor 2b); HER2 : récepteur 2 du facteur de croissance épidermique (human epidermal growth factor receptor 2); MSI : instabilité microsatellitaire (microsatellite instability); PD-L1 : ligand de mort cellulaire programmée 1 (programmed death-ligand 1).
INTRODUCTION
Au Canada, les estimations indiquent que la survie nette à 5 ans normalisée selon l’âge chez les patients ayant reçu un diagnostic de cancer de l’estomac est de 25 % (2008 à 2010).*,1

* Estimations de la survie nette après 5 ans, normalisées selon l’âge, pour les sièges primaires de cancer, pour les deux sexes; données combinées de 3 ans.
AU CANADA
Parmi les patients qui survivent au moins 1 an après leur diagnostic, environ 55 % survivent jusqu’à 5 ans après le diagnostic (2015 à 2017)†,2.
55% survivent jusqu’à 5 ans après le diagnostic
En 2022, il a été estimé que 4 100 nouveaux cas de cancer gastrique seraient diagnostiqués au Canada (excluant le Québec)3.
4 100 NOUVEAUX CAS
† Personnes de 15 à 99 ans au Canada (excluant le Québec).
DANS LE MONDE
Plus de 1 million de nouveaux cas de cancer gastrique/cancer de la JOG ont été diagnostiqués dans le monde en 2020, ce qui en fait le 5e cancer le plus diagnostiqué4.
Environ 769 000 personnes sont décédées des suites d’un cancer gastrique/cancer de la JOG dans le monde en 2020, ce qui en fait le 4e cancer le plus mortel4.
En 2018, le taux de survie globale à 5 ans dans le monde était d’environ ≤ 10 % dans les cas de cancer gastrique métastatique5.
BIOMARQUEURS EXPÉRIMENTAUX
BIOMARQUEURS CONNUS
Les biomarqueurs expérimentaux et les biomarqueurs connus peuvent être détectés par des méthodes standards de coloration par IHC.
BIOMARQUEURS EXPÉRIMENTAUX
CLDN18.2:
IHC8
FGFR2b:
IHC, ADNtc§,11,15
§ La surexpression de FGFR2b peut être établie par IHC; l’amplification du gène FGFR2 peut être déterminée par ADNtc11,15.
BIOMARQUEURS CONNUS
PD-L1:
IHC||,6
HER2:
IHC, HIS, SNG¶,6,16
MSI/MMR:
PCR/SNG, IHC6
ADNtc : ADN tumoral circulant; IHC : immunohistochimie; HIS : hybridation in situ (in situ hybridization); MMR : réparation des mésappariements (mismatch repair); SNG : séquençage de nouvelle génération; PCR : amplification en chaîne par polymérase (polymerase chain reaction).
|| Différents tests diagnostiques17.
¶ Autres méthodes d’HIS (CISH : HIS chromogénique [chromogenic ISH]; DDISH : HIS double couleur et double haptène [dual-color dual-hapten ISH]; FISH : HIS en fluorescence [fluorescent ISH]; SISH : HIS argentique [silver ISH])16.
Les biomarqueurs expérimentaux sont prévalents parmi les biomarqueurs du cancer gastrique/cancer de la JOG métastatique.
Les estimations de la prévalence des biomarqueurs issues de certaines études internationales sont présentées ci-dessous. Les données sur la prévalence peuvent varier d’une étude à l’autre en raison de l’hétérogénéité des tumeurs et des différences dans les populations de patients, la méthodologie des essais cliniques et les tests diagnostiques utilisés8,12,18–21.
BIOMARQUEURS EXPÉRIMENTAUX
CLDN18.28
(forte expression)
29 % des cas primaires
34 % des métastases ganglionnaires
FGFR2b18
(surexpression)#
3 à 61 %
# La surexpression a été déterminée par IHC18.
BIOMARQUEURS CONNUS
PD-L119,20
(variable en raison de nombreux facteurs)**
CPS ≥ 1: 67 à 73 %
CPS ≥ 5: 29 à 31 %
CPS ≥ 10: 16 à 18 %
HER212
(positif)
22 %
MSI21
(élevée)
4 %
CPS : score positif combiné (combined positive score).
** La prévalence de PD-L1 à différents seuils de CPS a été explorée19.

CLDN18.2
Les claudines sont une famille de protéines transmembranaires9,22 :
Les claudines sont des composantes majeures des jonctions serrées épithéliales et endothéliales, qui participent au contrôle du flux de molécules entre les cellules7-9.
Les claudines sont présentes partout dans le corps, mais deux isoformes spécifiques de CLDN18 se retrouvent dans certains types de tissus9,22 :
Des études précliniques ont montré que la CLDN18.2 pourrait être exposée dans les tumeurs gastriques9.
CONFINÉE DANS LES TISSUS SAINS

Dans les cellules épithéliales gastriques, la CLDN18.2 est habituellement enfouie dans le complexe supramoléculaire de la jonction serrée8,9.
Elle régule les propriétés des barrières sélectives et contribue à l’adhérence entre les cellules de l’épithélium8,9.
CONSERVÉE PENDANT LA TRANSFORMATION


La CLDN18.2 demeure présente pendant la transformation maligne, tant dans le siège de la tumeur primaire que dans la maladie métastatique23.
La CLDN18.2 peut aussi être exprimée lorsqu’une tumeur se développe dans les tissus du pancréas, des poumons et des ovaires9.
Une étude internationale a montré que la CLDN18.2 était exprimée dans environ 62 % des cancers gastriques primaires et 55 % des métastases ganglionnaires (à tout niveau), et qu’environ 29 % et 34 % des patients, respectivement, avaient obtenu un résultat positif à CLDN18.2 (forte expression)*,8.
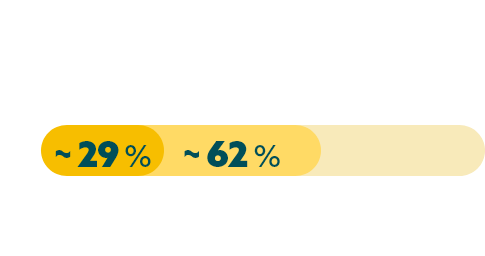



* La population à l’étude se limitait à 523 patients atteints d’un cancer gastrique (n = 408) ou d’un cancer de la jonction œsogastrique (n = 115), dont 195 présentaient une forte expression de CLDN18.28.
Lors de l’évaluation de la relation entre la CLDN18.2 et les autres biomarqueurs, les données d’une étude internationale indiquent que le chevauchement est limité.
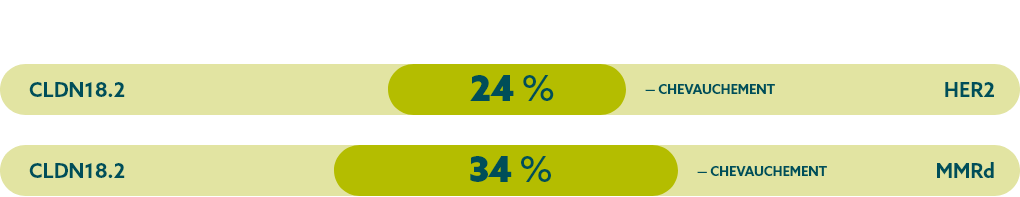



* La population à l’étude se limitait à 523 patients atteints d’un cancer gastrique (n = 408) ou d’un cancer de la jonction œsogastrique (n = 115), dont 195 présentaient une forte expression de CLDN18.2. Le FGFR2b n’a pas été évalué dans cette étude8.
MMRd : déficience du système de réparation des mésappariements (mismatch repair deficient)
La CLDN18.2 est exprimée dans les tumeurs de type diffus et dans les tumeurs de type intestinal8.

FGFR2b
La signalisation de FGFR entre en jeu dans la mitogenèse, la différenciation, la prolifération cellulaire, l’angiogenèse et l’invasion10.
Une surexpression de FGFR2b a été signalée chez jusqu’à 15 % des cas de cancer gastrique/cancer de la JOG métastatique, et une positivité de FGFR2b a été observée dans 3 à 61 % des cas.*,18 Ces données ont été rapportées dans une étude internationale.
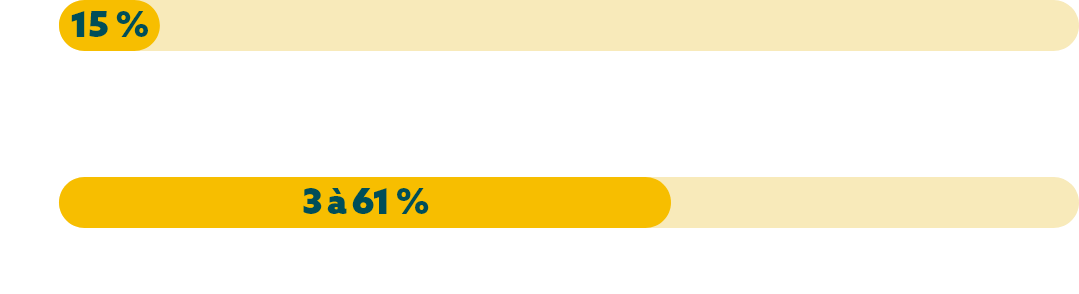

* Positivité de FGFR2b : surexpression (IHC) et/ou amplification du gène.
Il est possible de détecter la surexpression de FGFR2b à l’aide des tests suivants11,15.

HER2
Le HER2 (récepteur 2 du facteur de croissance épidermique humain) est un récepteur à activité tyrosine kinase qui est surexprimé et/ou amplifié chez les personnes atteintes d’un cancer gastrique/cancer de la JOG métastatique6,10.
Dans une étude internationale, la positivité de HER2 a été rapportée dans 22 % des cas de cancer gastrique/cancer de la JOG au stade avancé12.


Positivité de HER2 : surexpression (IHC3+) et/ou amplification du gène (analyse par FISH positive)
Le HER2 peut être détecté par IHC, par des méthodes d’HIS et par SNG, et est généralement davantage associé aux tumeurs de type intestinal*,6,12,16.
* L’IHC et l’HIS doivent être réalisées en premier, puis une analyse supplémentaire par SNG peut être effectuée au besoin6.
MSI
La MSI est associée à une instabilité génomique et à une susceptibilité accrue au développement tumoral10.
Les microsatellites sont des séquences répétées de nucléotides dans l’ADN13.
Dans une étude internationale, une MSI élevée a été rapportée dans 4 % des cas de cancer gastrique/cancer de la JOG métastatique21.


La MSI est habituellement détectée par diverses méthodes6.

PD-L1
Le PD-L1 (ligand de mort cellulaire programmée 1) est une protéine transmembranaire qui peut s’exprimer sur diverses cellules tumorales et/ou cellules immunitaires28.
Dans diverses études internationales, la prévalence de PD-L1 a été rapportée pour plusieurs seuils de positivité : CPS ≥ 1 : 67 à 73 %; CPS ≥ 5 : 29 à 31 %; CPS ≥ 10 : 16 à 18 %*,†,19,20.






* La population à l’étude se limitait à 592 patients atteints d’un cancer gastrique/cancer de la JOG localement avancé ou métastatique, dont la maladie avait progressé après un traitement de première intention à base de platine et de fluoropyrimidine20.
† L’étude a analysé 56 échantillons de biopsies provenant de patients allemands atteints d’un adénocarcinome gastrique principalement non métastatique qui n’avaient jamais été traités ou qui avaient reçu un traitement néoadjuvant19.
L’expression de PD-L1 est détectée par IHC6.
RÉSUMÉ
Les lignes directrices de pratique clinique en oncologie du NCCN sur le cancer gastrique appuient l’analyse des biomarqueurs6.
Les lignes directrices du NCCN recommandent :
L’analyse des biomarqueurs permet une meilleure compréhension de la physiopathologie du cancer gastrique/cancer de la JOG métastatique, car de plus en plus de biomarqueurs sont découverts.
* L’IHC et l’HIS doivent être réalisées en premier, puis une analyse supplémentaire par SNG peut être effectuée au besoin6.
La poursuite des recherches sur les biomarqueurs élargit notre vision de la population de patients et révèle plus d’informations sur la physiopathologie du cancer gastrique/cancer de la JOG métastatique.
Télécharger un document PDF sur les avancées en matière de biomarqueurs dans les cas de cancer gastrique/cancer de la JOG métastatique.
RÉFÉRENCES
L’information contenue sur le site gastriccancerbiomarkers.ca est destinée aux résidents du Canada.
© 2023 Astellas Pharma Canada, Inc. Tous droits réservés.
CONDITIONS D’UTILISATION DU SITE WEB (entrée en vigueur : 04/23)
ATTENTION: VEUILLEZ LIRE ATTENTIVEMENT CES CONDITIONS AVANT D’UTILISER LE SITE WEB GASTRICCANCERBIOMARKERS.CA. EN UTILISANT CE SITE, Y COMPRIS TOUT SERVICE OFFERT SUR GASTRICCANCERBIOMARKERS.CA OU PAR L’INTERMÉDIAIRE DE CELUI-CI (« services »), VOUS INDIQUEZ QUE VOUS ACCEPTEZ CES CONDITIONS. SI VOUS N’ACCEPTEZ PAS CES CONDITIONS, VEUILLEZ VOUS ABSTENIR D’UTILISER CE SITE.
Astellas Pharma Canada, Inc., (Astellas) peut en tout temps réviser les présentes conditions d’utilisation en mettant à jour ce document; il vous est donc conseillé de consulter à intervalles réguliers les conditions d’utilisation en vigueur, que vous êtes tenu de respecter. Certaines dispositions de ces conditions d’utilisation peuvent être remplacées par des avis juridiques ou des conditions expressément désignés situés sur certaines pages de ce site Web. Les conditions d’utilisation sont accessibles en tout temps à GastricCancerBiomarkers.ca.
INFORMATION GÉNÉRALE. Le présent site Web contient de l’information qui pourrait intéresser les membres du secteur des soins de santé. N’hésitez pas à consulter ce site Web et les services qui y sont associés. L’accès à ce site Web et son utilisation sont soumis aux conditions d’utilisation suivantes et à toutes les lois applicables. En accédant à ce site Web et en consultant ses services, vous acceptez sans restriction ni réserve les présentes conditions d’utilisation, et vous reconnaissez qu’elles ont préséance sur toute autre entente intervenue entre vous et Astellas.
CONFIDENTIALITÉ. Les politiques d’Astellas sur l’utilisation de vos renseignements personnels sont présentées dans la politique de confidentialité d’Astellas, à laquelle vous pouvez accéder ici, et qui est intégrée par renvoi au présent document. En utilisant le présent site Web et tout service fourni sur ce site ou par l’intermédiaire de celui-ci (services), vous libérez Astellas de toute responsabilité en lien avec la collecte, l’utilisation ou la divulgation d’information, tel qu’il est décrit dans la politique de confidentialité d’Astellas.
CONTENU DU SITE. Tout le contenu du site Web, y compris le texte, les images, les figures, les documents, le contenu audio et le contenu vidéo (collectivement, le « contenu du site ») est protégé par les lois applicables en matière de droits d’auteur. Vous pouvez copier, télécharger ou imprimer le contenu du site pour votre usage personnel et non commercial seulement, mais toute modification ou autre reproduction est interdite. Il est autrement interdit de copier, télécharger, reproduire, supprimer, modifier, republier, retransmettre, afficher ou utiliser le contenu du site pour en créer une œuvre dérivée sans l’autorisation écrite d’Astellas.
Les marques de commerce, marques de service, présentations commerciales, logos, concepts et slogans qui apparaissent sur ce site Web sont la propriété d’Astellas, de ses sociétés affiliées, de ces concédants de licence ou de ses partenaires, et ne peuvent pas être utilisés à des fins promotionnelles ou publicitaires, ou pour indiquer toute affiliation avec Astellas ou approbation par Astellas, sans l’autorisation écrite expresse de la part d’Astellas.
Rien sur ce site Web ne saurait être interprété comme un octroi de tout permis ou droit d’utiliser toute marque de commerce, tout brevet ou droit d’auteur d’Astellas ou d’un tiers.
Vous avez l’entière responsabilité de tout contenu, y compris le texte, les photographies, les caricatures, les illustrations, les concepts, les icônes, les articles ou les enregistrements audio et vidéo (collectivement, le « contenu généré par les utilisateurs ») que vous publiez, envoyez par courriel ou transmettez de toute autre manière par l’intermédiaire de ce site Web. Le contenu généré par les utilisateurs n’est pas la propriété d’Astellas, et Astellas n’approuve aucun contenu généré par les utilisateurs qui est publié ou transmis par l’intermédiaire de ce site, et elle ne garantit pas l’exactitude, l’intégrité ou la qualité d’un tel contenu. Toute information que vous transmettez par l’intermédiaire du présent site Web ou autrement à Astellas par courriel, à l’exception des renseignements permettant de vous identifier directement tels qu’ils sont définis dans la politique de confidentialité d’Astellas, sera considérée comme non confidentielle, et Astellas n’aura aucune obligation de quelque nature que ce soit à l’égard de cette information et sera libre de la reproduire, de l’utiliser, de la divulguer et de la distribuer à d’autres sans limite. Astellas est libre d’utiliser tout concept, idée, savoir-faire ou technique contenu dans cette information à toute fin que ce soit, ce qui inclut des activités de développement, de fabrication et de marketing.
Le contenu ou le matériel du site Web est fourni par Astellas à titre d’information seulement. Rien sur ce site Web ne pourra être considéré comme un conseil (médical, juridique, financier, d’investissement ou autre conseil professionnel) ou comme une recommandation, et l’information contenue sur le site Web ne doit pas être utilisée pour fonder une décision ou une action. Le présent site Web ne vise pas à faire la promotion d’un produit ou d’un traitement, ni à influencer les décisions d’achat, de prescription ou de diagnostic.
OBLIGATIONS DES VISITEURS OU UTILISATEURS DU SITE. Vous acceptez de vous abstenir des actions suivantes lorsque vous visitez le site Web ou utilisez tout service offert sur ce site ou par l’intermédiaire de celui-ci :
Astellas peut, à son entière discrétion, prendre toute mesure jugée nécessaire, y compris mettre fin à votre accès au site Web ou modifier le contenu généré par des utilisateurs si Astellas croit que le comportement ou le contenu d’un utilisateur ne respecte pas les présentes conditions d’utilisation ou pourrait créer un fardeau pour Astellas, ses partenaires, ses fournisseurs ou toute autre partie ou personne. Astellas n’aura aucune responsabilité envers vous ou tout tiers en lien avec cet arrêt de votre utilisation ou cette modification. Les présentes conditions d’utilisation survivront à tout arrêt de votre utilisation et modification du contenu.
LIENS VERS D’AUTRES SITES WEB. Uniquement pour votre commodité, Astellas peut fournir sur son site Web des liens vers d’autres sites Web qu’elle ne détient pas et ne contrôle pas. En utilisant ces liens, vous quitterez le présent site Web. N’oubliez pas que les liens mènent vers des sites qui ne sont pas nécessairement la propriété d’Astellas, et que l’information qui y est contenue pourrait changer sans qu’Astellas ne le sache. Les liens vers les sites de tiers et leur contenu ne peuvent pas être attribués à Astellas (ou à l’une de ses filiales) de quelque manière que ce soit. Astellas n’a pas tenté de vérifier la véracité et l’exactitude des sites tiers et de leur contenu, et n’affirme ou ne garantit aucunement qu’ils soient vrais ou exacts. Si vous décidez d’accéder aux sites de tiers par les liens présentés sur le présent site Web, vous le faites à vos propres risques. Si Astellas approuve une organisation précise, une mention l’indiquera clairement à côté du lien menant vers cette organisation.
EXCLUSION DE GARANTIES. CE SITE WEB, Y COMPRIS TOUT MATÉRIEL, INFORMATION OU SERVICE OFFERT SUR CELUI-CI OU PAR L’INTERMÉDIAIRE DE CELUI-CI, EST FOURNI « TEL QUEL » ET « TEL QUE DISPONIBLE ». AINSI, DANS LES LIMITES PERMISES PAR LA LOI, ASTELLAS DÉCLINE EXPRESSÉMENT TOUTE GARANTIE, EXPLICITE OU IMPLICITE, Y COMPRIS TOUTE GARANTIE DE VALEUR COMMERCIALE, DE CORRESPONDANCE À UN USAGE DONNÉ, OU D’ABSENCE DE CONTREFAÇON. DE PLUS, ASTELLAS NE GARANTIT PAS L’EXACTITUDE OU L’EXHAUSTIVITÉ DE L’INFORMATION CONTENUE SUR CE SITE ET PEUT APPORTER DES CHANGEMENTS À L’INFORMATION, AUX SERVICES OU AU MATÉRIEL RENDUS DISPONIBLES SUR LE SITE WEB OU PAR L’INTERMÉDIAIRE DE CELUI-CI À TOUT MOMENT ET SANS AVIS PRÉALABLE AUX UTILISATEURS DU SITE WEB. L’INFORMATION CONTENUE SUR CE SITE WEB QUI EST ACTUALISÉE PÉRIODIQUEMENT POURRAIT NE PAS ÊTRE À JOUR AU MOMENT DE VOTRE VISITE DU SITE ET POURRAIT CONTENIR DES ERREURS. ASTELLAS NE GARANTIT PAS QUE LE SITE WEB RÉPONDRA À VOS EXIGENCES, QU’IL SERA TOUJOURS DISPONIBLE, SÉCURITAIRE, LIBRE D’ERREURS OU ACCESSIBLE RAPIDEMENT; QUE LES MESSAGES OU DEMANDES SERONT TRANSMIS; QUE LES PROBLÈMES SERONT CORRIGÉS; OU QUE LE SITE WEB EST LIBRE DE VIRUS OU D’AUTRES ÉLÉMENTS NUISIBLES. ASTELLAS N’OFFRE AUCUNE GARANTIE QUANT AUX BIENS OU SERVICES ACHETÉS OU OBTENUS PAR L’INTERMÉDIAIRE DU SITE OU QUANT À TOUTE TRANSACTION AMORCÉE PAR L’INTERMÉDIAIRE DU SITE. VOUS ASSUMEZ L’ENSEMBLE DES RISQUES QUANT AUX RÉSULTATS ET À LA PERFORMANCE DU SITE ET QUANT À TOUT BIEN OU SERVICE QUE VOUS AVEZ ACHETÉ SUR LE SITE.
LIMITATION DE RESPONSABILITÉ. EN AUCUN CAS ASTELLAS NE SERA TENUE RESPONSABLE DE DOMMAGES QUELS QU’ILS SOIENT. CELA INCLUT, SANS S’Y LIMITER, LES DOMMAGES DIRECTS, INDIRECTS, ACCESSOIRES, PUNITIFS ET CONSÉCUTIFS (NOTAMMENT CEUX RÉSULTANT D’UNE PERTE DE PROFITS, D’UNE PERTE DE DONNÉES OU D’UNE INTERRUPTION DES AFFAIRES) DÉCOULANT DE L’UTILISATION DU PRÉSENT SITE WEB OU DE L’INCAPACITÉ À L’UTILISER, DES SITES WEB LIÉS À CE SITE, DU MATÉRIEL OU DE L’INFORMATION CONTENU SUR CES SITES, OU DE TOUT MATÉRIEL, PRODUIT OU SERVICE OFFERT SUR LE PRÉSENT SITE OU LES SITES WEB LIÉS À CE SITE, QU’ILS SOIENT BASÉS SUR UNE GARANTIE, UN CONTRAT, UN ACTE DÉLICTUEL, OU TOUTE AUTRE THÉORIE JURIDIQUE, INDÉPENDAMMENT DU FAIT QU’ASTELLAS AIT ÉTÉ AVISÉE DE LA POSSIBILITÉ DE TELS DOMMAGES OU NON. EN AUCUN CAS ASTELLAS, SES FOURNISSEURS OU TOUTE AUTRE PARTIE IMPLIQUÉE DANS LA CRÉATION, LA PRODUCTION OU LA MISE EN LIGNE DU PRÉSENT SITE WEB NE SERA RESPONSABLE ENVERS VOUS DE QUELQUE MANIÈRE QUE CE SOIT POUR QUELQUE DÉCISION PRISE OU ACTION OU NON ACTION POSÉE SUR LA BASE DE L’INFORMATION FOURNIE SUR CE SITE WEB. LES LOIS APPLICABLES POURRAIENT NE PAS PERMETTRE L’EXCLUSION OU LA LIMITATION DES DOMMAGES ACCESSOIRES OU CONSÉCUTIFS; DANS CE CAS, LES LIMITATIONS OU EXCLUSIONS CI-DESSUS POURRAIENT NE PAS S’APPLIQUER À VOUS.
CE SITE WEB EST RÉSERVÉ AUX CANADIENS. L’accès au présent site Web et son utilisation sont sujets aux conditions d’utilisation décrites ci-dessus. Ce site Web a été développé et est maintenu par Astellas. L’information, les textes et les énoncés sont réservés aux résidents du Canada.